Інсулін в бодібілдингу

http://sportwiki.to
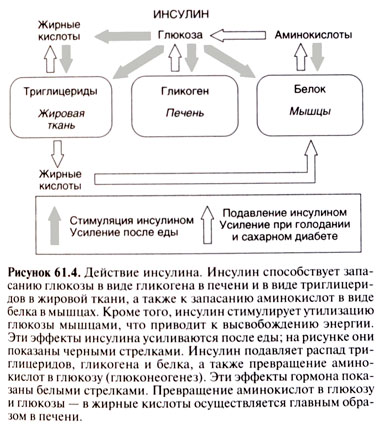
Фізіологічна дія
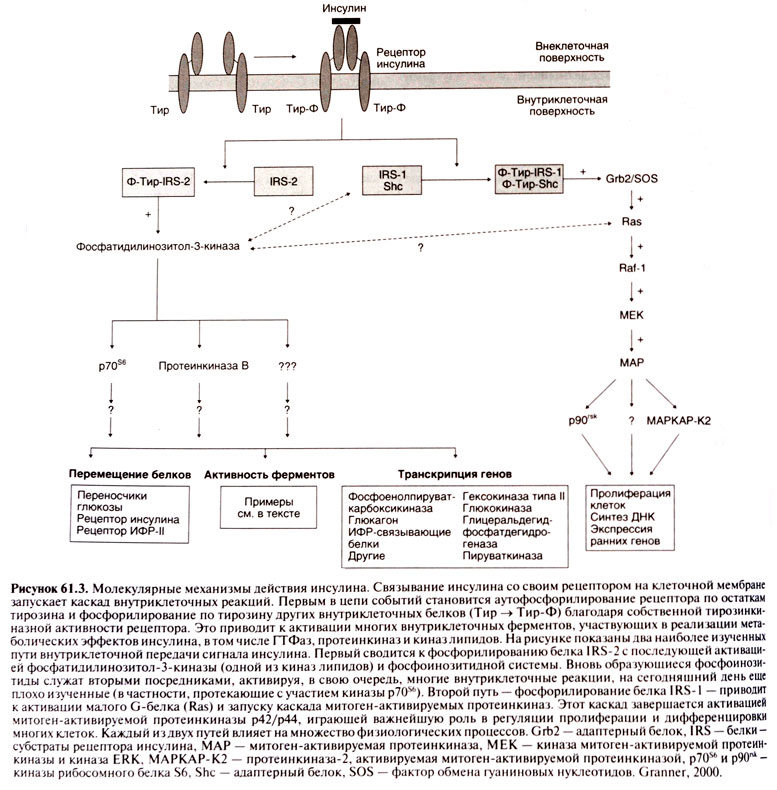
Малюнок 61.3. Молекулярні механізми дії інсуліну. http://sportwiki.to
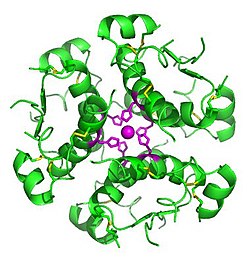
Інсулін, Матеріал з Вікіпедії - вільної енциклопедії
опис
http://www.rlsnet.ru
Інсулін (від лат. Insula - острівець) є білково-пептидних гормоном, що виробляється β-клітинами острівців Лангерганса підшлункової залози. У фізіологічних умовах в β-клітинах інсулін утворюється з препроінсуліну - одноланцюжкові білка-попередника, що складається з 110 амінокислотних залишків. Після перенесення через мембрану шорсткого ЕПР від препроінсуліну отщепляется сигнальний пептид з 24 амінокислот і утворюється проінсулін. Довгий ланцюг проінсуліну в апараті Гольджі упаковується в гранули, де в результаті гідролізу отщепляются чотири основних амінокислотних залишку з утворенням інсуліну і С-кінцевого пептиду (фізіологічна функція С-пептиду невідома).
Молекула інсуліну складається з двох поліпептидних ланцюгів. Одна з них містить 21 амінокислотний залишок (ланцюг А), друга - 30 амінокислотних залишків (ланцюг В). Ланцюги з'єднані двома дисульфідними містками. Третій дисульфідних місток сформований всередині ланцюга А. Загальна молекулярна маса молекули інсуліну - близько 5700. Амінокислотна послідовність інсуліну вважається консервативною. У більшості видів є один ген інсуліну, який кодує один білок. Виняток становлять щури і миші (мають по два гена інсуліну), у них утворюються два інсуліну, що відрізняються двома амінокислотними залишками В-ланцюга.
Первинна структура інсуліну у різних біологічних видів, в т.ч. і у різних ссавців, дещо різниться. Найбільш близький до структури інсуліну людини - свинячий інсулін, який відрізняється від людського однією амінокислотою (у нього в ланцюзі У замість залишку амінокислоти треоніну міститься залишок аланіну). Бичачий інсулін відрізняється від людського трьома амінокислотними залишками.
Історична довідка. У 1921 р Фредерік Г. Бантінг і Чарльз Г. Бест, працюючи в лабораторії Джона Дж. Р. Маклеода в Університеті Торонто, виділили з підшлункової залози екстракт (як пізніше з'ясувалося, що містить аморфний інсулін), який знижував рівень глюкози в крові у собак з експериментальним цукровим діабетом. У 1922 р екстракт підшлункової залози ввели першому пацієнту - 14-річному Леонарду Томпсону, хворому на діабет, і тим самим врятували йому життя. У 1923 р Джеймс Б. Колліпом розробив методику очищення екстракту, який виділяється з підшлункової залози, що в подальшому дало змогу одержувати з підшлункової залоз свиней та великої рогатої худоби активні екстракти, що дають відтворювані результати. У 1923 р Бантінг і Маклеод за відкриття інсуліну були удостоєні Нобелівської премії з фізіології і медицині. У 1926 р Дж. Абель і В. Дю-Віньо отримали інсулін в кристалічному вигляді. У 1939 р інсулін був вперше схвалений FDA (Food and Drug Administration). Фредерік Сенгер повністю розшифрував амінокислотну послідовність інсуліну (1949-1954 рр.) У 1958 р Сенгер була присуджена Нобелівська премія за роботи по розшифровці структури білків, особливо інсуліну. У 1963 р був синтезований штучний інсулін. Перший рекомбінантний людський інсулін був схвалений FDA в 1982 р Аналог інсуліну ультракороткої дії (інсулін лізпро) був схвалений FDA в 1996 р
Механізм дії. У реалізації ефектів інсуліну провідну роль відіграє його взаємодія зі специфічними рецепторами, що локалізуються на плазматичній мембрані клітини, і освіту інсулін-рецепторного комплексу. У комплексі з інсуліновим рецептором інсулін проникає в клітину, де впливає на процеси фосфорилювання клітинних білків і запускає численні внутрішньоклітинні реакції.
У ссавців інсулінові рецептори знаходяться практично на всіх клітинах - як на класичних клітинах-мішенях інсуліну (гепатоцити, міоцити, ліпоціти), так і на клітинах крові, головного мозку і статевих залоз. Число рецепторів на різних клітинах коливається від 40 (еритроцити) до 300 тис. (Гепатоцити і ліпоціти). Рецептор інсуліну постійно синтезується і розпадається, час його напіввиведення становить 7-12 год.
Рецептор інсуліну являє собою великий трансмембранний глікопротеїн, що складається з двох α-субодиниць з молекулярною масою 135 кДа (кожна містить 719 або 731 амінокислотний залишок в залежності від сплайсингу мРНК) і двох β-субодиниць з молекулярною масою 95 кДа (по 620 амінокислотних залишків). Субодиниці з'єднані між собою дисульфідними зв'язками і утворюють гетеротетрамерную структуру β-α-α-β. Альфа-субодиниці розташовані внеклеточно і містять ділянки, що зв'язують інсулін, будучи розпізнає частиною рецептора. Бета-субодиниці утворюють трансмембранний домен, мають тірозінкіназной активністю і виконують функцію перетворення сигналу. Зв'язування інсуліну з α-субодиницями інсулінового рецептора призводить до стимуляції тірозінкіназной активності β-субодиниць шляхом аутофосфорілірованію їх тирозинових залишків, відбувається агрегація α, β-гетеродімери і швидка интернализация гормон-рецепторних комплексів. Активоване рецептор інсуліну запускає каскад біохімічних реакцій, в т.ч. фосфорилирование інших білків усередині клітини. Першою з таких реакцій є фосфорилювання чотирьох білків, званих субстратами рецептора інсуліну (insulin receptor substrate), - IRS-1, IRS-2, IRS-3 і IRS-4.
Фармакологічні ефекти інсуліну. Інсулін впливає практично на всі органи і тканини. Однак його головними мішенями служать печінку, м'язова і жирова тканина.
Ендогенний інсулін - найважливіший регулятор вуглеводного обміну, екзогенний - специфічне цукрознижуючу засіб. Вплив інсуліну на вуглеводний обмін пов'язано з тим, що він підсилює транспорт глюкози через клітинну мембрану і її утилізацію тканинами, сприяє перетворенню глюкози в глікоген в печінці. Інсулін, крім того, пригнічує ендогенну продукцію глюкози за рахунок придушення гликогенолиза (розщеплення глікогену до глюкози) і глюконеогенезу (синтез глюкози з невуглеводних джерел - наприклад з амінокислот, жирних кислот). Крім гіпоглікемічного, інсулін надає ряд інших ефектів.
Вплив інсуліну на жировий обмін проявляється в пригніченні ліполізу, що призводить до зниження надходження вільних жирних кислот в кровотік. Інсулін перешкоджає утворенню кетонових тіл в організмі. Інсулін посилює синтез жирних кислот і їх подальшу естеріфікаціі.
Інсулін бере участь в метаболізмі білків: збільшує транспорт амінокислот через клітинну мембрану, стимулює синтез пептидів, зменшує витрату тканинами білка, гальмує перетворення амінокислот в кетокислот.
Дія інсуліну супроводжується активацією або пригніченням ряду ферментів: стимулюються глікогенсинтетазу, піруват-дегидрогеназа, гексокіназа, відзначено зниження ліпази (і гідролізу ліпіди жирової тканини, і липопротеин-ліпаза, яка зменшує «помутніння» сироватки крові після прийому багатою жирами їжі).
В фізіологічної регуляції біосинтезу і секреції інсуліну підшлунковою залозою головну роль грає концентрація глюкози в крові: при підвищенні її змісту секреція інсуліну посилюється, при зниженні - сповільнюється. На секрецію інсуліну, крім глюкози, впливають електроліти (особливо іони Ca2 +), амінокислоти (в т.ч. лейцин і аргінін), глюкагон, соматостатин.
Фармакокінетика. Препарати інсуліну вводять п / к, в / м або в / в (в / в вводять тільки інсуліни короткої дії і тільки при діабетичної прекомі і комі). Не можна вводити в / в суспензії інсуліну. Температура введеного інсуліну повинна відповідати кімнатній, тому що холодний інсулін всмоктується повільніше. Найбільш оптимальним способом для постійної інсулінотерапії в клінічній практиці є п / к введення.
Повнота всмоктування і початок ефекту інсуліну залежать від місця введення (зазвичай інсулін вводять в область живота, стегна, сідниці, верхню частину рук), дози (обсягу введеного інсуліну), концентрації інсуліну в препараті і ін.
Швидкість всмоктування інсуліну в кров з місця п / к введення залежить від ряду факторів - типу інсуліну, місця ін'єкції, швидкості місцевого кровотоку, місцевої м'язової активності, кількості введеного інсуліну (в одне місце рекомендується вводити не більше 12-16 ОД препарату). Швидше за все інсулін надходить у кров з підшкірної клітковини передньої черевної стінки, повільніше - з області плеча, передньої поверхні стегна і ще повільніше - з подлопаточной області і сідниці. Це пов'язано зі ступенем васкуляризації підшкірної жирової клітковини перерахованих областей. Профіль дії інсуліну схильний до значних коливань як у різних людей, так і у одного і того ж людини.
У крові інсулін зв'язується з альфа-і бета-глобулінами, в нормі - 5-25%, але зв'язування може зростати при лікуванні через появу сироваткових антитіл (вироблення антитіл до екзогенного інсуліну призводить до інсулінорезистентності; при використанні сучасних високоочищених препаратів інсулінорезистентність виникає рідко ). T1 / 2 з крові становить менше 10 хв. Велика частина надійшов в кровотік інсуліну піддається протеолитическому розпаду в печінці та нирках. Швидко виводиться з організму нирками (60%) і печінкою (40%); менше 1,5% виводиться з сечею в незміненому вигляді.
Препарати інсуліну, які застосовуються в даний час, відрізняються по ряду ознак, в т.ч. за джерелом походження, тривалості дії, pH розчину (кислі і нейтральні), наявністю консервантів (фенол, крезол, фенол-крезол, метилпарабен), концентрацією інсуліну - 40, 80, 100, 200, 500 ОД / мл.
Класифікація. Інсуліни зазвичай класифікують за походженням (бичачий, свинячий, людський, а також аналоги людського інсуліну) і тривалості дії.
Залежно від джерел отримання розрізняють інсуліни тваринного походження (головним чином препарати свинячого інсуліну), препарати інсуліну людини напівсинтетичні (отримують з свинячого інсуліну методом ферментативної трансформації), препарати інсуліну людини генно-інженерні (ДНК-рекомбінантні, одержувані методом генної інженерії).
Для медичного застосування інсулін раніше отримували в основному з підшлункової залоз великої рогатої худоби, потім з підшлункової залоз свиней, враховуючи, що свинячий інсулін ближчий до інсуліну людини. Оскільки бичачий інсулін, що відрізняється від людського трьома амінокислотами, досить часто викликає алергічні реакції, на сьогоднішній день він практично не застосовується. Свинячий інсулін, що відрізняється від людського однією амінокислотою, рідше викликає алергічні реакції. В лікарських препаратах інсуліну при недостатній очищення можуть бути присутніми домішки (проінсулін, глюкагон, соматостатин, білки, поліпептиди), здатні викликати різні побічні реакції. Сучасні технології дозволяють отримувати очищені (монопіковие - хроматографически очищені з виділенням «піку» інсуліну), високоочищені (монокомпонентні) і кристалізовані препарати інсуліну. З препаратів інсуліну тваринного походження перевага віддається монопіковие інсуліну, що отримується з підшлункової залози свиней. Одержуваний методами генної інженерії інсулін повністю відповідає амінокислотним складом інсуліну людини.
Активність інсуліну визначають біологічним методом (за здатністю знижувати вміст глюкози в крові у кроликів) або фізико-хімічним методом (шляхом електрофорезу на папері або методом хроматографії на папері). За одну одиницю дії, або міжнародну одиницю, приймають активність 0,04082 мг кристалічного інсуліну. Підшлункова залоза людини містить до 8 мг інсуліну (приблизно 200 ОД).
Препарати інсуліну за тривалістю дії поділяють на препарати короткої та ультракороткої дії - імітують нормальну фізіологічну секрецію інсуліну підшлунковою залозою у відповідь на стимуляцію, препарати середньої тривалості і препарати тривалої дії - імітують базальну (фонову) секрецію інсуліну, а також комбіновані препарати (поєднують обидві дії) .
Розрізняють такі групи:
Інсуліни ультракороткої дії (гіпоглікемічний ефект розвивається через 10-20 хв після п / к введення, пік дії досягається в середньому через 1-3 год, тривалість дії становить 3-5 год):
- інсулін лізпро (Хумалог);
- інсулін аспарт (НовоРапід Пенфилл, НовоРапід ФлексПен);
- інсулін глулізін (Апідра).
Інсуліни короткої дії (початок дії зазвичай через 30-60 хв; максимум дії через 2-4 год; тривалість дії до 6-8 ч):
- інсулін розчинний [людський генно-інженерний] (Актрапід hм, Генсулін Р, Рінсулін Р, Хумулін Регуляр);
- інсулін розчинний [людський напівсинтетичний] (Біогулін Р, Хумодар Р);
- інсулін розчинний [свинячий монокомпонентний] (Актрапід МС, Монодар, Моносуінсулін МК).
Препарати інсуліну пролонгованої дії - включають в себе препарати середньої тривалості дії і препарати тривалої дії.
Інсуліни середньої тривалості дії (початок через 1,5-2 год; пік через 3-12 год; тривалість 8-12 год):
- інсулін-ізофан [людський генно-інженерний] (Біосулін Н, Гансулін Н, Генсулін Н, Інсуман база ГТ, Інсуран НПХ, Протафан НМ, Рінсулін НПХ, Хумулін НПХ);
- інсулін-ізофан [людський напівсинтетичний] (Біогулін Н, Хумодар Б);
- інсулін-ізофан [свинячий монокомпонентний] (Монодар Б, Протафан МС);
- інсулін-цинк суспензія складова (Монотард МС).
Інсуліни тривалої дії (початок через 4-8 год; пік через 8-18 год; загальна тривалість 20-30 год):
- інсулін гларгин (Лантус);
- інсулін детемір (Левемір Пенфилл, ФлексПен).
Препарати інсуліну комбінованої дії (біфазної препарати) (гіпоглікемічний ефект починається через 30 хв після п / к введення, досягає максимуму через 2-8 год і триває до 18-20 год):
- інсулін двофазний [людський напівсинтетичний] (Біогулін 70/30, Хумодар K25);
- інсулін двофазний [людський генно-інженерний] (Гансулін 30р, Генсулін М 30, Інсуман Комб 25 ГТ, Мікстард 30 НМ, Хумулін М3);
- інсулін аспарт двофазний (НовоМікс 30 Пенфилл, НовоМікс 30 ФлексПен).
Інсуліни ультракороткої дії - аналоги інсуліну людини. Відомо, що ендогенний інсулін в β-клітинах підшлункової залози, а також молекули гормону в випускаються розчинах інсуліну короткого дії полімеризовані і являють собою гексамери. При п / к введенні гексамерние форми всмоктуються повільно і пік концентрації гормону в крові, аналогічний такому у здорової людини після їжі, створити неможливо. Першим коротко чинним аналогом інсуліну, який всмоктується з підшкірної клітковини в 3 рази швидше, ніж людський інсулін, був інсулін лізпро. Інсулін лізпро - похідне людського інсуліну, отримане шляхом перестановки двох амінокислотних залишків в молекулі інсуліну (лізин і пролін в положеннях 28 і 29 В-ланцюга). Модифікація молекули інсуліну порушує утворення гексамеров і забезпечує швидке надходження препарату в кров. Майже відразу після п / к введення в тканинах молекули інсуліну лізпро у вигляді гексамеров швидко дисоціюють на мономери і надходять в кров. Інший аналог інсуліну - інсулін аспарт - був створений шляхом заміни пролина в положенні В28 на негативно заряджену аспарагиновую кислоту. Подібно до інсуліну лізпро, після п / к введення він також швидко розпадається на мономери. В інсуліні глулізіне заміщення амінокислоти аспарагін людського інсуліну в позиції В3 на лізин і лізину у позиції В29 на глутамінову кислоту також сприяє більш швидкій абсорбції. Аналоги інсуліну ультракороткої дії можна вводити безпосередньо перед прийомом їжі або після їжі.
Інсуліни короткої дії (їх називають також розчинними) - це розчини в буфері з нейтральними значеннями pH (6,6-8,0). Вони призначені для підшкірного, рідше - введення. При необхідності їх вводять також внутрішньовенно. Вони надають швидке і відносно нетривалий гіпоглікемічну дію. Ефект після підшкірної ін'єкції настає через 15-20 хв, досягає максимуму через 2 год; загальна тривалість дії становить приблизно 6 год. Ними користуються в основному в стаціонарі в ході встановлення необхідної для хворого дози інсуліну, а також коли потрібно швидкий (ургентний) ефект - при діабетичної коми і прекомі. При в / в введенні T1 / 2 становить 5 хв, тому при діабетичної кетоацидотической комі інсулін вводять в / в крапельно. Препарати інсуліну короткої дії застосовують також як анаболічних засобів та призначають, як правило, в малих дозах (по 4-8 ОД 1-2 рази на день).
Інсуліні середньої трівалості Дії гірше розчінні, повільніше всмоктуються з підшкірної клітковіні, внаслідок чого ма ють більш трівалім ефектом. Трівала дія ціх препаратів досягається наявністю спеціального пролонгатора - протаміну (ізофан, протафан, базал) або цинку. Уповільнення всмоктування інсуліну в препаратах, що містять інсулін цинк суспензію складових, обумовлено наявністю крісталів цинку. НПХ-інсулін (нейтральний протамін Хагедорна, або ізофан) являє собою суспензію, що складається з інсуліну і протаміну (протамін - білок, ізольований з молочка риб) в стехиометрическом співвідношенні.
До інсуліни тривалої дії відноситься інсулін гларгин - аналог людського інсуліну, отриманий методом ДНК-рекомбінантної технології - перший препарат інсуліну, який не має вираженого піку дії. Інсулін гларгин отримують шляхом двох модифікацій в молекулі інсуліну: заміною в позиції 21 А-ланцюга (аспарагін) на гліцин і приєднанням двох залишків аргініну до С-кінця У-ланцюга. Препарат являє собою прозорий розчин з рН 4. Кислий рН стабілізує гексамери інсуліну і забезпечує тривале і передбачуване всмоктування препарату з підшкірної клітковини. Однак через кислого рН інсулін гларгин не можна комбінувати з інсулінами короткої дії, які мають нейтральний рН. Одноразове введення інсуліну гларгіну забезпечує 24-годинний безпіковий глікемічний контроль. Більшість препаратів інсуліну мають т.зв. «Піком» дії, що святкується, коли концентрація інсуліну в крові досягає максимуму. Інсулін гларгин не володіє вираженим піком, оскільки вивільняється в кровотік з відносно постійною швидкістю.
Препарати інсуліну пролонгованої дії випускаються в різних лікарських формах, що надають гіпоглікемічний ефект різної тривалості (від 10 до 36 год). Пролонгований ефект дозволяє зменшити число щоденних ін'єкцій. Випускаються вони зазвичай у вигляді суспензій, що вводяться тільки підшкірно або внутрішньом'язово. При діабетичній комі і прекоматозний стан пролонговані препарати не застосовують.
Комбіновані препарати інсуліну є суспензії, що складаються з нейтрального розчинного інсуліну короткої дії та інсуліну-ізофан (середньої тривалості дії) в певних співвідношеннях. Таке поєднання інсулінів різної тривалості дії в одному препараті дозволяє позбавити пацієнта від двох ін'єкцій при роздільному використанні препаратів.
Показання. Основним показанням до застосування інсуліну є цукровий діабет типу 1, однак у певних умовах його призначають і при цукровому діабеті типу 2, в т.ч. при резистентності до пероральних гіпоглікемічних засобів, при важких супутніх захворюваннях, при підготовці до оперативних втручань, діабетичної коми, при діабеті у вагітних. Інсуліни короткої дії застосовують не тільки при цукровому діабеті, а й при деяких інших патологічних процесах, наприклад, при загальному виснаженні (як анаболічного засобу), фурункульозі, тиреотоксикозі, при захворюваннях шлунка (атонія, гастроптоз), хронічному гепатиті, початкових формах цирозу печінки , а також при деяких психічних захворюваннях (введення великих доз інсуліну - т.зв. гіпоглікемічна кома); іноді він використовується як компонент «поляризують» розчинів, використовуваних для лікування гострої серцевої недостатності.
Інсулін є основним специфічним засобом терапії цукрового діабету. Лікування цукрового діабету проводиться за спеціально розробленими схемами з використанням препаратів інсуліну різної тривалості дії. Вибір препарату залежить від тяжкості та особливостей перебігу захворювання, загального стану хворого і від швидкості настання і тривалості цукрознижувальної дії препарату.
Всі препарати інсуліну застосовуються за умови обов'язкового дотримання дієтичного режиму з обмеженням енергетичної цінності їжі (від 1700 до 3000 ккал).
При визначенні дози інсуліну керуються рівнем глікемії натщесерце і протягом доби, а також рівнем глюкозурії протягом доби. Остаточний підбір дози проводиться під контролем зниження гіперглікемії, глюкозурії, а також загального стану хворого.
Протипоказання. Інсулін протипоказаний при захворюваннях і станах, що протікають з гіпоглікемією (наприклад инсулинома), при гострих захворюваннях печінки, підшлункової залози, нирок, виразці шлунка і дванадцятипалої кишки, декомпенсованих вадах серця, при гострій коронарній недостатності та деяких інших захворюваннях.
Застосування при вагітності. Основним медикаментозним методом лікування цукрового діабету під час вагітності є інсулінотерапія, яка проводиться під ретельним контролем. При цукровому діабеті типу 1 продовжують лікування інсуліном. При цукровому діабеті типу 2 скасовують пероральні гіпоглікемічні засоби та проводять дієтотерапію.
Гестаційний цукровий діабет (діабет вагітних) - це порушення вуглеводного обміну, вперше виникло під час вагітності. Гестаційний цукровий діабет супроводжується підвищеним ризиком перинатальної смертності, частоти вроджених вад, а також ризиком прогресування діабету через 5-10 років після пологів. Лікування гестаційного цукрового діабету починають з дієтотерапії. При неефективності дієтотерапії застосовують інсулін.
Для пацієнток з раніше наявним або гестаційним цукровим діабетом важливо протягом всієї вагітності підтримувати адекватну регуляцію метаболічних процесів. Потреба в інсуліні може зменшуватися в I триместрі вагітності і збільшуватися в II-III триместрах. Під час пологів і безпосередньо після них потреба в інсуліні може різко знизитися (зростає ризик розвитку гіпоглікемії). У цих умовах важливе значення має ретельний контроль вмісту глюкози в крові.
Інсулін не проникає через плацентарний бар'єр. Однак материнські IgG-антитіла до інсуліну проходять через плаценту і, ймовірно, можуть викликати гіперглікемію у плода за рахунок нейтралізації секретується у нього інсуліну. З іншого боку, небажана дисоціація комплексів інсулін-антитіло може привести до гіперінсулінемії і гіпоглікемії у плода або новонародженого. Показано, що перехід з препаратів бичачого / свинячого інсуліну на монокомпонентні препарати супроводжується зниженням титру антитіл. У зв'язку з цим при вагітності рекомендують використовувати тільки препарати інсуліну людини.
Аналоги інсуліну (як і інші недавно розроблені засоби) з обережністю призначають при вагітності, хоча достовірних даних про несприятливу дію немає. Відповідно до загальновизнаних рекомендацій FDA (Food and Drug Administration), що визначають можливість застосування ЛЗ при вагітності, препарати інсулінів за дією на плід відносяться до категорії B (вивчення репродукції на тваринах не виявило несприятливої дії на плід, а адекватних і строго контрольованих досліджень у вагітних жінок не проведене), або до категорії C (вивчення репродукції на тваринах виявило несприятливу дію на плід, а адекватних і строго контрольованих досліджень у вагітних жінок не проведене, проте потенційна користь, пов'язана із застосуванням ЛЗ у вагітних, може виправдовувати його використання, незважаючи на можливий ризик). Так, інсулін лізпро відноситься до класу B, а інсулін аспарт і інсулін гларгин - до класу C.
Ускладнення інсулінотерапії. Гіпоглікемія. Введення надто високих доз, а також недолік надходження з їжею вуглеводів можуть спричинити гіпоглікемічну стан, може розвинутися гіпоглікемічна кома із втратою свідомості, судомами і пригніченням серцевої діяльності. Гіпоглікемія може також розвинутися у зв'язку з дією додаткових чинників, які збільшують чутливість до інсуліну (наприклад надниркових залоз, гіпопітуїтаризм) або збільшують захоплення глюкози тканинами (фізичне навантаження).
До ранніх симптомів гіпоглікемії, які в значній мірі пов'язані з активацією симпатичної нервової системи (адренергічна симптоматика) відносяться тахікардія, холодний піт, тремтіння, з активацією парасимпатичної системи - сильний голод, нудота, а також відчуття поколювання в області губ і язика. При перших ознаках гіпоглікемії необхідно проведення термінових заходів: хворий повинен випити солодкого чаю чи з'їсти кілька шматків цукру. При гіпоглікемічної коми в вену вводять 40% розчин глюкози в кількості 20-40 мл і більше, поки хворий не вийде з коматозного стану (зазвичай не більше 100 мл). Зняти гіпоглікемію можна також внутрім'язовим або підшкірним введенням глюкагону.
Збільшення маси тіла при інсулінотерапії пов'язано з усуненням глюкозурии, збільшенням реальної калорійності їжі, підвищенням апетиту і стимуляцією липогенеза під дією інсуліну. При дотриманні принципів раціонального харчування цього побічного ефекту можна уникнути.
Застосування сучасних високоочищених препаратів гормону (особливо генно-інженерних препаратів людського інсуліну) відносно рідко призводить до розвитку інсулінорезистентності та явищ алергії, однак такі випадки не виключені. Розвиток гострої алергічної реакції вимагає проведення негайної десенсибілізуючої терапії та заміни препарату. При розвитку реакції на препарати бичачого / свинячого інсуліну слід замінити їх препаратами інсуліну людини. Місцеві та системні реакції (свербіж, локальна або системна висип, утворення підшкірних вузликів в місці ін'єкції) пов'язані з недостатнім очищенням інсуліну від домішок або з застосуванням бичачого або свинячого інсуліну, що відрізняються по амінокислотної послідовності від людського.
Найчастіші алергічні реакції - шкірні, опосередковувані IgE-антитілами. Зрідка спостерігаються системні алергічні реакції, а також інсулінорезистентність, опосередковувані IgG-антитілами.
Порушення зору. Минущі порушення рефракції ока виникають на самому початку інсулінотерапії і проходять самостійно через 2-3 тижні.
Набряки. У перші тижні терапії виникають також минущі набряки ніг в зв'язку з затримкою рідини в організмі, т.зв. інсулінові набряки.
До місцевих реакцій відносять липодистрофию в місці повторних ін'єкцій (рідкісне ускладнення). Виділяють ліпоатрофії (зникнення відкладень підшкірного жиру) і ліпогіпертрофію (збільшення відкладення підшкірного жиру). Ці два стани мають різну природу. Ліпоатрофія - імунологічна реакція, обумовлена головним чином введенням погано очищених препаратів інсуліну тваринного походження, в даний час практично не зустрічається. Ліпогіпертрофія розвивається і при використанні високоочищених препаратів людського інсуліну і може виникати при порушенні техніки введення (холодний препарат, потрапляння спирту під шкіру), а також внаслідок анаболічного місцевої дії самого препарату. Ліпогіпертрофія створює косметичний дефект, що є проблемою для пацієнтів. Крім того, через це дефекту порушується всмоктування препарату. Для попередження розвитку ліпогіпертрофіі рекомендується постійно міняти місця ін'єкцій в межах однієї області, залишаючи відстань між двома проколами не менше 1 см.
Можуть відзначатися такі місцеві реакції, як біль у місці введення.
Взаємодія. Препарати інсуліну можна комбінувати один з одним. Багато ЛЗ можуть викликати гіпо- або гіперглікемію, або змінювати реакцію хворого на цукровий діабет на лікування. Слід враховувати взаємодію, можливе при одночасному застосуванні інсуліну з іншими лікарськими засобами. Альфа-адреноблокатори і бета-адреноміметики збільшують секрецію ендогенного інсуліну і посилюють дію препарату. Гіпоглікемічна дія інсуліну підсилюють пероральні гіпоглікемічні засоби, саліцилати, інгібітори МАО (включаючи фуразолідон, прокарбазин, селегілін), інгібітори АПФ, бромокриптин, октреотид, сульфаніламіди, анаболічні стероїди (особливо оксандролон, метандіенон) і андрогени (підвищують чутливість тканин до інсуліну і збільшують резистентність тканин до глюкагону, що і призводить до гіпоглікемії, особливо в разі інсулінорезистентності; може знадобитися зниження дози інсуліну), аналоги соматостатину, гуанетидин, ДІЗО пірамід, клофібрат, кетоконазол, препарати літію, мебендазол, пентамідин, піридоксин, пропоксифен, фенілбутазон, флуоксетин, теофілін, фенфлурамин, препарати літію, препарати кальцію, тетрациклін. Хлорохін, хінідин, хінін знижують деградацію інсуліну і можуть підвищувати концентрацію інсуліну в крові і збільшувати ризик гіпоглікемії.
Інгібітори карбоангідрази (особливо ацетазоламид), стимулюючи панкреатичні β-клітини, сприяють вивільненню інсуліну і підвищують чутливість рецепторів і тканин до інсуліну; хоча одночасне використання цих ЛЗ з інсуліном може підвищувати гіпоглікемічну дію, ефект може бути непередбачуваним.
Цілий ряд ЛЗ викликають гіперглікемію у здорових людей і посилюють перебіг захворювання у хворих на цукровий діабет. Гіпоглікемічна дія інсуліну послаблюють: антиретровірусні ЛЗ, аспарагиназа, пероральні гормональні контрацептиви, глюкокортикоїди, діуретики (тіазидні, етакринова кислота), гепарин, антагоністи Н2-рецепторів, сульфінпіразон, трициклічніантидепресанти, добутамін, ізоніазид, кальцитонін, ніацин, симпатоміметики, даназол, клонідин, БКК, діазоксид, морфін, фенітоїн, соматотропін, тиреоїдні гормони, похідні фенотіазину, нікотин, етанол.
Глюкокортикоїди і адреналін надають на периферичні тканини ефект, протилежний інсуліну. Так, тривалий прийом системних глюкокортикоїдів може викликати гіперглікемію, аж до цукрового діабету (стероїдний діабет), який може спостерігатися приблизно у 14% пацієнтів, що приймають системні кортикостероїди протягом декількох тижнів або при тривалому застосуванні топічних кортикостероїдів. Деякі ЛЗ інгібують секрецію інсуліну безпосередньо (фенітоїн, клонідин, дилтіазем) або за рахунок зменшення запасів калію (діуретики). Тиреоїдні гормони прискорюють метаболізм інсуліну.
Найбільш значимо і часто впливають на дію інсуліну бета-адреноблокатори, пероральні гіпоглікемічні засоби, глюкокортикоїди, етанол, саліцилати.
Етанол пригнічує глюконеогенез в печінці. Цей ефект спостерігається у всіх людей. У зв'язку з цим слід мати на увазі, що зловживання алкогольними напоями на тлі інсулінотерапії може привести до розвитку важкого гіпоглікемічного стану. Невеликі кількості алкоголю, прийнятого разом з їжею, зазвичай не викликають проблем.
Бета-адреноблокатори можуть пригнічувати секрецію інсуліну, змінювати метаболізм вуглеводів і збільшувати периферичну резистентність до дії інсуліну, що призводить до гіперглікемії. Однак вони можуть також пригнічувати дію катехоламінів на глюконеогенез і глікогеноліз, що пов'язане з ризиком важких гіпоглікемічних реакцій у хворих на цукровий діабет. Більш того, будь-який з бета-блокаторів може маскувати адренергическую симптоматику, викликану зниженням рівня глюкози в крові (в т.ч. тремор, серцебиття), порушуючи тим самим своєчасне розпізнавання пацієнтом гіпоглікемії. Селективні бета 1 адреноблокатори (в т.ч. ацебутолол, атенолол, бетаксолол, бісопролол, метопролол) виявляють ці ефекти в меншій мірі.
НПЗЗ та високі дози саліцилатів пригнічують синтез простагландину Е (який пригнічує секрецію ендогенного інсуліну) і підсилюють таким чином базальну секрецію інсуліну, підвищують чутливість β-клітин підшлункової залози до глюкози; гіпоглікемічний ефект при одночасному застосуванні може зажадати коригування дози НПЗЗ саліцілатів і / або інсуліну, особливо при тривалому спільному використанні.
В даний час випускається значна кількість інсулінових препаратів, в т.ч. отриманих з підшлункової залоз тварин і синтезованих методами генної інженерії. Препаратами вибору для проведення інсулінотерапії є генно-інженерні високоочищені людські інсуліни, що володіють мінімальної антигенностью (иммуногенной активністю), а також аналоги людського інсуліну.
Препарати інсуліну випускаються в скляних флаконах, герметично закупорених гумовими пробками з алюмінієвою обкаткою, в спеціальних т.зв. інсулінових шприцах або шприц-ручках. При користуванні шприц-ручок препарати перебувають в спеціальних флаконах-картриджах (Пенфілл).
Розробляються інтраназальні форми інсуліну і препарати інсуліну для прийому всередину. При комбінації інсуліну з детергентом і введенні у вигляді аерозолю на слизову оболонку носа ефективний рівень в плазмі досягається так само швидко, як і при в / в болюсному. Препарати інсуліну для інтраназального і перорального застосування знаходяться на стадії розробки або проходять клінічні випробування.
**













