Гіпермаркет знань >> хімія >> Хімія 9 клас >> Хімія: Алюміній
Будова і властивості атомів. Алюміній Аl - елемент головної підгрупи III групи періодичної системи Д. І. Менделєєва. Атом алюмінію містить на зовнішньому енергетичному рівні три електрони, які він легко віддає при хімічних взаємодіях. У родоначальника підгрупи і верхнього сусіда алюмінію - бору радіус атома менше (у бору він дорівнює 0,080 нм, у алюмінію - 0,143 нм). Крім того, у атома алюмінію з'являється один проміжний восьміелектрон-ний шар (2е-; 8е-; зе-), який перешкоджає тяжінню зовнішніх електронів до ядра. Тому у атомів алюмінію відновні властивості виражені набагато сильніше, ніж у атомів бору, який проявляє неметалічні властивості.
Майже у всіх своїх сполуках алюміній має ступінь окислення +3.
Алюміній - проста речовина. Сріблясто-білий легкий метал. Плавиться при 660 ° С. Дуже пластичний, легко витягується в дріт і прокочується в фольгу товщиною 0,01 мм. Володіє дуже великий електричну провідність і теплопровідність. Утворює з іншими металами легкі і міцні сплави.
Алюміній - дуже активний метал . В ряді напруг він знаходиться відразу ж після лужних і лужноземельних металів. Однак при кімнатній температурі на повітрі алюміній не змінюється, оскільки його поверхня покрита дуже міцною тонкою плівкою оксиду, яка захищає метал від впливу компонентів повітря і води.
Якщо порошок алюмінію або тонку алюмінієву фольгу сильно нагріти, то вони спалахують і згоряють сліпучим полум'ям:
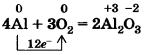
Дану реакцію ви спостерігаєте при горінні бенгальських вогнів і феєрверків.
Алюміній, як і всі метали, легко реагує з неметаллами , Особливо в порошкоподібному стані. Для того щоб почалася реакція, необхідно початкове нагрівання, за винятком реакцій з галогенами - хлором і бромом, зате потім все реакції алюмінію з неметалами йдуть дуже бурхливо і супроводжуються виділенням великої кількості теплоти: 
Алюміній добре розчиняється в розбавлених сірчаної і соляної кислотах:
2Аl + 6НСl = 2АlСl3 + ЗН2
2Аl + ЗН2SO4 = Аl2 (SO4) 3 + ЗН2
А ось концентровані сірчана і азотна кислоти пасивують алюміній, утворюючи на поверхні металу щільну, міцну оксидну плівку, яка перешкоджає подальшому протіканню реакції. Тому ці кислоти перевозять в алюмінієвих цистернах.
Як ви вже знаєте, оксид і гідроксид алюмінію мають амфотерними властивостями, тому алюміній розчиняється у водних розчинах лугів, утворюючи солі - алюмінати:
2Аl + 2NаОН + 2Н20 = 2NаАlO2 + ЗН2
Алюміній широко використовується в металургії для отримання металів - хрому, марганцю, ванадію, титану, цирконію з їх оксидів. Як ви пам'ятаєте, цей спосіб носить назву алюминотермии. На практиці часто застосовується терміт - суміш Fе3O4 з порошком алюмінію. Якщо цю суміш підпалити, наприклад, за допомогою магнієвої стрічки, то відбувається енергійна реакція з виділенням великої кількості теплоти.
Теплоти, що виділяється цілком достатньо для повного розплавлення утворюється заліза, тому цей процес використовують для зварювання сталевих виробів.
Алюміній дуже міцно пов'язаний в природних з'єднаннях з киснем та іншими елементами, і виділити його з цих сполук хімічними методами дуже важко. Алюміній можна отримати електролізом - розкладанням розплаву його оксиду Аl2O3 на складові частини за допомогою електричного струму. Але температура плавлення оксиду алюмінію близько 2050 ° С, тому для проведення електролізу необхідні великі витрати енергії.
Технічно доступним металом алюміній став після того, як був знайдений спосіб знизити температуру плавлення оксиду алюмінію хоча б до 1000 ° С. Цей спосіб відкрили в 1886 р американський і французький вчені Ч. Хол і П. Еру, які встановили, що оксид алюмінію добре розчиняється в розплавленому кріоліті, формула якого Nа3АlF6. Розплав оксиду алюмінію в кріоліті піддають електролізу на алюмінієвих заводах.
Світове виробництво алюмінію стає дедалі більше. Він відтіснив на третє і наступні місця мідь та інші кольорові метали і став другим за значенням металом триваючого залізного віку . Алюміній майже втричі легше стали і стійкий до корозії, тому вигідніше стали в тих областях застосування, де потрібні ці властивості.
З'єднання алюмінію. У природі алюміній зустрічається тільки у вигляді сполук і за поширеністю в земній корі займає перше місце серед металів і третє - серед всіх елементів (після кисню і кремнію). Загальний вміст алюмінію в земній корі становить близько 9% (по масі).
Зазначимо найважливіші природні сполуки алюмінію.
Алюмосилікати. Ці сполуки можна розглядати як солі, утворені оксидами алюмінію, кремнію, лужних і лужноземельних металів. Вони і складають основну масу земної кори. Зокрема, алюмосилікати входять до складу польових шпатів - найбільш поширених мінералів і глин.
Боксит - гірська порода, з якої отримують алюміній. Вона містить оксид алюмінію Аl2O3.
Корунд - мінерал складу Аl2O3, володіє дуже високою твердістю, його дрібнозернистий різновид, що містить домішки, - наждак, застосовується як абразивний (шліфувальний) матеріал.
Цю ж формулу має і інше природне з'єднання - глинозем.
Добре відомі прозорі забарвлені домішками кристали корунду: червоні - рубіни і сині - сапфіри, які використовують як дорогоцінні камені. В даний час їх отримують штучно і застосовують не тільки для прикрас, але і для технічних цілей, наприклад, для виготовлення деталей годинників та інших точних приладів. Кристали рубінів застосовують в лазерах.
Оксид алюмінію Аl2O3 - біла речовина з дуже високою температурою плавлення. Може бути отриманий розкладанням при нагріванні відповідного йому гідроксиду алюмінію:
2Аl (ОН) 3 = А12O3 + ЗН2O
Гідроксид алюмінію Аl (ОН) 3 випадає у вигляді драглистого осаду при дії лугів на розчини солей алюмінію, наприклад:
АlСl3 + ЗNaОН = Аl (ОН) 3 + ЗNaСl
надлишок
Як амфотерний гідроксид він легко розчиняється в кислотах і в розчинах лугів:
Аl (ОН) 3 + ЗНNO3 = Аl (NО3) 3 + ЗН20
Алюминатами називають солі нестійких алюмінієвих кислот - ортоалюмініевой і метаалюминиевой (її можна розглядати як ортоалюмініевую кислоту, від молекули якої відняли молекулу води). До природних алюмінатом відноситься благородна шпінель (вона прикрашає історичну реліквію - корону російських імператорів) і дорогоцінний хризоберил.
Солі алюмінію, крім фосфатів, добре розчинні у воді. Деякі солі (сульфіди, сульфіти) розкладаються водою.
Хлорид алюмінію АlСl3 застосовують як каталізатор у виробництві дуже багатьох органічних речовин.
Відкриття алюмінію. Алюміній був вперше отриманий датським фізиком X. Ерстед в 1825 р Назва цього елемента походить від лат. Алюмен, так в давнину називалися галун, які використовували для фарбування тканин.
1. Будова атома алюмінію.
2 Фізичні та хімічні властивості алюмінію: освіта броміду, сульфіду, карбіду, оксиду, алюмінатів.
3. Алюмінотермія.
4. Отримання алюмінію електролізом.
5. Області застосування алюмінію.
6. Природні сполуки алюмінію: алюмосилікати (глина і польові шпати), корунд (рубін, сапфір, наждак).
7. Амфотерность оксиду і гідроксиду алюмінію.
Чому в алюмінієвому посуді не можна зберігати лужні або кислі розчини?
Яке з'єднання алюмінію могло послужити матеріалом для гіперболоїда інженера Гаріна в романі А. Толстого ?
Яку хімічну реакцію поклав в основу оповідання «Бенгальські вогні» його автор Н. Носов?
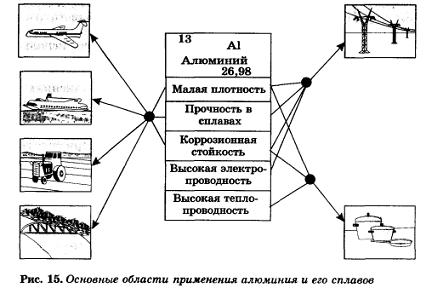
На яких фізичних і хімічних властивостях грунтується застосування в техніці алюмінію і його сплавів?
Напишіть в іонному вигляді рівняння реакцій між розчинами сульфату алюмінію і гідроксиду калію при нестачі і надлишку останнього.
Напишіть рівняння реакцій наступних перетворень: Аl -> АlСl3 -> Аl (0Н) 3 -> Аl2O3 -> NаАl02 -> Аl2 (SO4) 3 -> Аl (ОН) 3 -> АlСl3 -> NаАlO2
Реакції, що відбуваються за участю електролітів, запишіть в іонної формі. Першу реакцію розгляньте як окислювально-відновний процес.
Який об'єм водню може бути отриманий при розчиненні в едком натре 270 мг сплаву алюмінію, що містить міді? Вихід водню прийміть рівним 85% від тео-іческі можливого.
Напишіть твір на тему «Художній образ веществаа або хімічного процесу», використовуючи свої знання з хімії алюмінію.
графіки і таблиці до уроку хімії 9 класу , Ідеальні уроки з хімії , Програма по усіх предметів
зміст уроку  конспект уроку
конспект уроку
опорний каркас  презентація уроку
презентація уроку  акселеративного методи
акселеративного методи  інтерактивні технології Практика
інтерактивні технології Практика  завдання і вправи
завдання і вправи  самоперевірка
самоперевірка  практикуми, тренінги, кейси, квести
практикуми, тренінги, кейси, квести  домашні завдання
домашні завдання  дискусійні питання
дискусійні питання  риторичні питання від учнів Ілюстрації
риторичні питання від учнів Ілюстрації  аудіо-, відео- та мультимедіа
аудіо-, відео- та мультимедіа  фотографії, картинки
фотографії, картинки  графіки, таблиці, схеми
графіки, таблиці, схеми  гумор, анекдоти, приколи, комікси
гумор, анекдоти, приколи, комікси  притчі, приказки, кросворди, цитати Доповнення
притчі, приказки, кросворди, цитати Доповнення  реферати
реферати  статті
статті  фішки для допитливих
фішки для допитливих  шпаргалки
шпаргалки  підручники основні і додаткові
підручники основні і додаткові  словник термінів
словник термінів  інші Удосконалення підручників та уроків
інші Удосконалення підручників та уроків  виправлення помилок в підручнику
виправлення помилок в підручнику  оновлення фрагмента в підручнику
оновлення фрагмента в підручнику  елементи новаторства на уроці
елементи новаторства на уроці  заміна застарілих знань новими Тільки для вчителів
заміна застарілих знань новими Тільки для вчителів  ідеальні уроки
ідеальні уроки  календарний план на рік
календарний план на рік  методичні рекомендації
методичні рекомендації  програми
програми  обговорення Інтегровані уроки
обговорення Інтегровані уроки
Якщо у вас є виправлення або пропозиції до даного уроку, Напишіть нам .
Якщо ви хочете побачити інші коригування та побажання до уроків, дивіться тут - освітній форум .
Чому в алюмінієвому посуді не можна зберігати лужні або кислі розчини?Носов?
На яких фізичних і хімічних властивостях грунтується застосування в техніці алюмінію і його сплавів?













