- Передмова
- Чи може внутрішньоутробний вплив глюкокортикоїдів бути причиною серцево-судинних і метаболічних захворювань...
- ВСТУП
- Епідеміологія
- ЕКСПЕРИМЕНТИ НА ТВАРИН
- РОЛЬ ГЛЮКОКОРТИКОЇДІВ
- ЯК ЗДІЙСНЮЄТЬСЯ програмування?
- Ренінангіотензинової СИСТЕМА
- ЦЕНТРАЛЬНА НЕРВОВА СИСТЕМА
- КЛІТИНИ підшлункової залози
- ДЕКСАМЕТАЗОН І нейростероідов
- ВИКОРИСТАННЯ ГЛЮКОКОРТИКОЇДІВ під час вагітності
- ПИТАННЯ, залишилися без відповіді
Передмова
Пропонуємо вашій увазі переклад статті з проблеми застосування глюкокортикоїдних гормонів під час вагітності. Навіть короткочасне призначення глюкокортикоїдів може на кілька десятиліть вперед "перепрограмувати" роботу функціональних систем плода та негативно вплинути на формування поведінки, контроль артеріального тиску і на регуляцію обміну речовин. Синтетичний гормон "обманює" організм плоду, імітуючи стресовий сигнал з боку організму матері, змушуючи плід завчасно форсувати мобілізацію резервів. В цьому суть негативної дії цих препаратів. Ця дія ще більш посилюється в результаті того, що сучасні "довгограючі" глюкокортикоїди (дексаметазон, метипред) не піддаються інактивує дії ферментних систем плаценти і надають тривалий вплив на органи і тканини-мішені. Надаючи імуносупресивну дію, ці препарати послаблюють організм вагітної жінки по відношенню до вірусних інфекцій.
Глюкокортикоїдних гормони повинні застосовуватися при вагітності тільки тоді, коли користь від їх застосування значно перевищує можливий ризик довготривалих негативних наслідків. До таких показань відноситься загроза передчасних пологів (глюкокортикоїди призначаються одноразово або у вигляді дуже короткого курсу і дозволяють значно поліпшити готовність недоношеної дитини до самостійного існування), активні аутоімунні і ревматичні захворювання (глюкокортикоїди дозволяють різко знизити ризик важких ускладнень у жінки) і вроджена внутрішньоутробна гіперплазія кори наднирників у плода (це спадкове захворювання, яке вимагає спеціальної антенатальної діагностики; застосування глюкокор ікоідов дозволяє уникнути вірілізації плода жіночої статі).
Автори нічого не пишуть про призначення глюкокортикостероїдів з метою збереження вагітності. І це не випадково. На Заході таке "лікування" було відкинуто ще в кінці 1950-х - початку 1960-х років, оскільки не існує вагомих доказів його ефективності. Розвиток сучасних методів діагностики і лікування невиношування вагітності, зокрема, в рамках імунології репродукції, не залишає місця подібної застарілої практики.
І. І. Гузов
Чи може внутрішньоутробний вплив глюкокортикоїдів бути причиною серцево-судинних і метаболічних захворювань в середньому віці?
Miodrag Dodic, Arianne Peers, John P. Coghlan, Marelyn Wintour - Trends in Endocrinology and Metabolism 1999 року, 10: 86-91
ВСТУП
Протягом багатьох років дослідження, що проводяться як на тварин, так і на людину, виявили залежність поведінки потомства від ступеня стресового стану матері і від впливу глюкокортикоїдів на плід в період внутрішньоутробного розвитку. За останні 10 років було отримано значну кількість переконливих епідеміологічних даних про те, що уповільнення розвитку плода в матці є дуже важливим фактором ризику виникнення серцево-судинних порушень і порушень обміну речовин в дорослому віці. Пізніше було показано, що дуже важливим, навіть ключовим, моментом подібної схильності є також вплив на плід надлишку глюкокортикоїдів. Навіть короткочасне (48 годин) застосування дексаметазону на ранніх термінах вагітності може призводити до постійного підвищення артеріального тиску у дорослих овець. Розуміння механізму подібного програмування і фізіологічних змін, що відбуваються при цьому, є однією з найактуальніших завдань сучасної ендокринології та біології розвитку.
Багато років визначальним фактором у розвитку неінфекційних захворювань у дорослому віці вважалося вплив несприятливих умов життя і наявність генетичної схильності. Пізніше було висунуто припущення про те, що найперша довкілля, матка, в період внутрішньоутробного розвитку людини, може грати навіть більш значиму роль, ніж кожен з перерахованих вище факторів. Це призвело до створення концепції "програмування", яка полягає у тому, що зміни внутрішньоутробної середовища, що виникають в певні, обмежені за часом періоди, може мати віддалені довготривалі наслідки і запускати ланцюг подій, що приводить до розвитку функціональних порушень у дорослому віці.
Концепція про вплив внутрішньоматкового оточення на подальшу долю потомства не так вже й нова. Однак раніше проведені дослідження в цій області більшу увагу приділяли впливу внутрішньоутробних впливів на поведінку новонародженого / підлітка / дорослого. І якщо відзначалися якесь відхилення, вони розглядалися як поведінково або психічно обумовлені. Були проведені роботи, присвячені зв'язку стану психічного здоров'я потомства з впливом великої кількості різноманітних "стресів", які долають вагітної. Ці "стреси" включали в себе багаторазове дія гучного раптового шуму (наприклад, на жінок, які проживають біля аеропортів) або проживання в країні, яка готується до війни, або веде війну (наприклад, 6-денна Ізраїльська війна). У цих випадках відзначалася затримка внутрішньоутробного розвитку плода, труднощі та / або уповільнення формування рухових, вербальних і соціальних навичок. Дослідження, що проводяться на тваринах, були в основному зосереджені на вивченні впливу ролі передбачуваних медіаторів цих порушень - глюкокортикоїдних гормонів надниркових залоз.
Епідеміологія
Близько десяти років тому епідеміологічні дослідження, проведені у Великобританії, стали виявляти взаємозв'язок між низькою вагою дитини при народженні і значним зростанням ризику розвитку патології серцево-судинної системи в дорослому віці (до 20% після 45 років). Надалі подібний взаємозв'язок була виявлена і для підвищеного ризику розвитку в дорослому віці порушень обміну речовин - цукрового діабету 2-го типу і дисліпідемії. Так звана "гіпотеза Баркера" полягає в тому, що недостатнє харчування жінки під час вагітності призводить до затримки внутрішньоутробного розвитку плода і запуску механізмів адаптації плода до недостатнього надходження необхідних поживних речовин. При цьому в фізіологічних системах плода виникають незворотні зміни, що призводять до розвитку патологічних станів у дорослому віці.
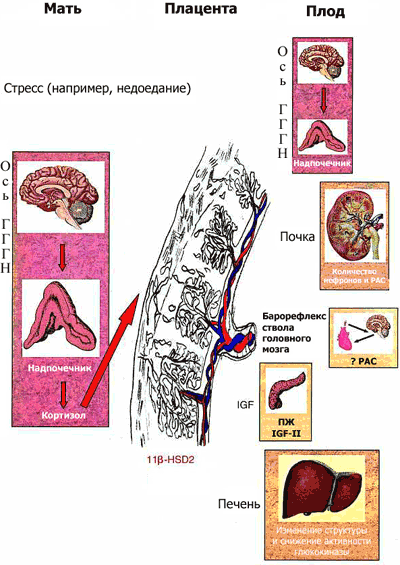 Мал. 1 Потенційні механізми "програмування плода" Стрес материнського організму (наприклад, недоїдання під час вагітності) призводить до активації осі гіпокамп-гіпоталамус-гіпофіз-надниркові залози (ГГГН) у вагітної, що, в свою чергу, в залежності від рівня активності ферменту плаценти, яка інактивує кортикостероїди (11 -гідроксістероіддегідрогенази 2-го типу, 11 HSD-2), призводить до впливу на плід високих концентрацій глюкокортикоїдів (ГК). Високий рівень глюкокортикоїдів в крові плода сприяє зміні числа стероїдних рецепторів в ГГГН системі, змінює рівень активності інших функціональних систем (гормон росту / інсулін-залежний фактор росту, ренін-ангіотензинової системи, викликає заміщення клітин підшлункової залози плода клітинами, характерними для дорослого організму ), що в кінцевому підсумку призводить до патологічних змін в дорослому віці. IGF II: інсуліноподібний фактор росту II; РАС: ренін-ангіотензинової системи; ПЖ: підшлункова залоза.
Мал. 1 Потенційні механізми "програмування плода" Стрес материнського організму (наприклад, недоїдання під час вагітності) призводить до активації осі гіпокамп-гіпоталамус-гіпофіз-надниркові залози (ГГГН) у вагітної, що, в свою чергу, в залежності від рівня активності ферменту плаценти, яка інактивує кортикостероїди (11 -гідроксістероіддегідрогенази 2-го типу, 11 HSD-2), призводить до впливу на плід високих концентрацій глюкокортикоїдів (ГК). Високий рівень глюкокортикоїдів в крові плода сприяє зміні числа стероїдних рецепторів в ГГГН системі, змінює рівень активності інших функціональних систем (гормон росту / інсулін-залежний фактор росту, ренін-ангіотензинової системи, викликає заміщення клітин підшлункової залози плода клітинами, характерними для дорослого організму ), що в кінцевому підсумку призводить до патологічних змін в дорослому віці. IGF II: інсуліноподібний фактор росту II; РАС: ренін-ангіотензинової системи; ПЖ: підшлункова залоза. До 1996 року взаємозв'язок між патологією серцево-судинної системи в дорослому віці і низькою вагою при народженні була виявлена в 34 дослідженнях, що охоплюють більш, ніж 60 000 спостережень. У роботах, що проводяться Barker і колегами, наводяться дані про те, що у людей, що народилися з масою тіла менше 2,5 кг, у віці 50 років і старше частота пульсу в спокої вище, ніж у людей, що важили при народженні 3,3 кг и більше. Це інтерпретувалося, як доказ впливу підвищеної активності симпатичної нервової системи, запрограмоване в періоді внутрішньоутробного розвитку. Також було показано, що навіть при наявності в спокої нормального розкиду значень кортизолу плазми, найвищі значення відзначаються у людей, що мають при народженні найнижчу масу тіла. Подібна взаємозв'язок була встановлена і відносно значень систолічного артеріального тиску, рівня тригліцеридів плазми, ступеня інсулінорезистентності.
ЕКСПЕРИМЕНТИ НА ТВАРИН
Експерименти, проведені на тваринах (морські свинки, щури, вівці), підтвердили взаємозв'язок між затримкою внутрішньоутробного розвитку і формуванням артеріальної гіпертензії або обмінних порушень в дорослому віці. Незалежно від причини, що приводить до порушення внутрішньоутробного розвитку у тварин (порушення маткового кровотоку, анемія у матері, недостатньо калорійне харчування, або нізкобелковую дієта під час вагітності), результат виходив один і той же. Потомство щурів, які отримували нізкобелковую дієту під час вагітності та лактації, мало істотні зміни в морфометрії печінки і значне зниження активності глюкокинази в перівенозних областях. В отриманому потомство морських свинок, що мали при народженні низьку масу тіла, у молодих дорослих самців розвивалася артеріальна гіпертензія, відзначалося зменшення обсягу м'язової тканини і збільшення жирової тканини, порушення толерантності до глюкози, порушений гомеостаз холестерину. Найцікавіше, що недостатнє харчування в першій половині вагітності у тварин з великою тривалістю вагітності, як, наприклад, вівці, призводило до народження потомства, у якого до 3-х місячного віку розвивалася артеріальна гіпертонія.
РОЛЬ ГЛЮКОКОРТИКОЇДІВ
Докази важливу роль глюкокортикоїдних гормонів в ембріональному програмуванні системних захворювань, що розвиваються в дорослому віці, були отримані з декількох джерел. Інтерес до цих сполук був викликаний переконливими даними про те, що глюкокортикоїди можуть безпосередньо приводити до підвищення артеріального тиску і формування інсулінорезистентності в дорослому віці, а вплив глюкокортикоїдів під час вагітності може уповільнювати розвиток плода і перенастроювати стан функціональної системи ГГГН в дорослому віці. Крім того, в експериментах на невагітних тварин було відзначено, що недостатнє харчування призводить до підвищення активності гіпокамп-гіпоталамо-гіпофізарно-надниркової системи. Подальші дослідження, що включають використання карбеноксолона (препарату, що приводить до придушення плацентарної інактивації глюкокортикоїдів), показали уповільнення внутрішньоутробного розвитку потомства і підвищення артеріального тиску в дорослому віці. Видалення наднирників у вагітних тварин з використанням під час вагітності тільки фізрозчину (0,9% NaCl) замість питної води, призводить до зниження ваги потомства при народженні, але не до підвищення артеріального тиску. При додаванні карбеноксолона до сольового розчину подальшого зниження ваги при народженні не відзначалося, також не було відзначено підвищення артеріального тиску. Використання метірапона у щурів протягом терміну вагітності 0-14 днів в поєднанні з низько-білкової дієтою призвело до народження потомства зі зниженим вагою, але з нормальним артеріальним тиском протягом 7 тижнів після народження. Заміна метірапона на кортикостерон привела до підвищення артеріального тиску після народження тільки у жіночих особин.
У багатьох дослідженнях використовувався синтетичний стероїд дексаметазон. Це було пов'язано з тим, що дексаметазон не береться інактивації ферментом 11 -гідроксістероіддегідрогенази 2-го типу (11 -HSD2). Дані дослідження становлять інтерес з точки зору визначення часу критичного періоду "програмування". Призначення вагітним щурам дексаметазону тільки протягом останньої третини гестаційного періоду привела до підвищення кров'яного тиску у потомства через 16 тижнів після народження. Призначення дексаметазону вагітним вівцям протягом всього лише двох днів в кінці першого місяця вагітності (яка триває 5 місяців) призводило до підвищення кров'яного тиску у ягнят з 3-х місячного віку. Підвищення кров'яного тиску не було, якщо дексаметазон призначався на початку 3-го місяця вагітності. Період призначення дексаметазону був настільки коротким, що зниження ваги при народженні не відбувалося. Це узгоджується з даними Hawkins, які показали, що недостатнє харчування овець тільки в першій половині вагітності призводить до програмування ягнят на підвищення кров'яного тиску до тримісячного віку. Таким чином, отримані результати показують, що критичні періоди "програмування" можливі як на ранніх, так і на пізніх етапах гестаційного періоду. Раніше це було показано для впливу андрогенів на формування специфічного для підлоги дозрівання нейро-ендокринної системи, але по відношенню до глюкокортикоїдів це дію тоді не вважалося вартим уваги.
ЯК ЗДІЙСНЮЄТЬСЯ програмування?
Теоретично у внутрішньоутробному періоді під впливом ряду несприятливих факторів можуть відбуватися зміни багатьох органів і систем плода, що призводять до довготривалих віддалених наслідків у дорослому віці.
Ренінангіотензинової СИСТЕМА
Функціональна система ренін-ангіотензин (ренін, ангіотензин, ангиотензинпревращающий фермент, рецептори 1-го і 2-го типів) бере участь в регуляції кров'яного тиску і представлена в багатьох органах плода (нирки, головний мозок, серцево-судинна система). Очевидна взаємозв'язок між ренінангіотензинової системою і функціональною системою підтримки рівня глюкози в плазмі крові. Було показано, що уповільнення внутрішньоутробного розвитку плода особливо несприятливо впливає на розвиток нирок, а саме у вигляді зменшення кількості нефронів в активний період нефрогенеза і більш високими, ніж в нормі, концентраціями реніну і ангіотензину II в крові пуповини. Внаслідок зменшення кількості нефронів підвищується ризик розвитку ниркової недостатності, що призводить до активізації ренінангіотензинової системи з метою збереження швидкості клубочкової фільтрації. Попередні дані участі ренінангіотензинової системи отримані в дослідженнях LGEdwards і співавт., Вказують на те, що у ягнят, народжених з низькою вагою в стані гіпоксії, кров'яний тиск підтримується на нормальному рівні за рахунок збільшення активності системи ренін-ангіотензин. Короткочасне (протягом 4 годин) введення каптоприлу, що приводить до зниження продукції ангіотензину II, викликає зниження кров'яного тиску у ягнят, народжених з низькою вагою, але не у нормальних ягнят. У потомства щурів, які отримували під час вагітності недостатня кількість поживних речовин, використання каптоприлу в період від 2 до 4 тижнів після народження запобігало розвиток артеріальної гіпертензії. У дослідженнях M. Dodic і співавт. у ягнят з артеріальною гіпертензією, що виникла внаслідок застосування дексаметазону на ранніх термінах вагітності, не було зареєстровано судинної реактивності до екзогенного ангіотензину II у віці 5 - 19 місяців. Проте, той факт, що ренін-ангіотензинової системи грає важливу роль в установці барорефлекса, необхідного для підтримки нормального кров'яного тиску, не піддається сумніву. У дослідженнях M. Dodic у овець з артеріальною гіпертонією, що розвилася в результаті призначення дексаметазону в ранні терміни вагітності, не було підвищеної судинної реактивності на екзогенне введення ангіотензину II у віці 5-19 місяців. Однак, ренін-ангіотензинової системи участвовует в налаштуванні барорефлекса, що забезпечує межі коливань артеріального тиску. M. Dodic і співавт. показали, що відмінність в значеннях кров'яного тиску між групами ягнят, що піддавалися і не піддавалися внутрішньоутробному дії дексаметазону, збільшується зі збільшенням віку ягнят, і барорефлексов в основній групі перенастраивается. Попередні результати, що показують, що показники серцевого викиду у цих овець вище, ніж у контрольній групі, добре узгоджуються з цією концепцією динаміки барорефлекса.
ЦЕНТРАЛЬНА НЕРВОВА СИСТЕМА
У проведених дослідженнях отримано велику кількість доказів, які б свідчили про те, що материнський стрес під час вагітності або вплив надлишку глюкокортикоїдів призводить до змін в структурах головного мозку плода (стовбур головного мозку, гіпокамп, гіпоталамус, неокортекс). У потомства щурів, які зазнали впливу дексаметазону на терміни 17-19 днів вагітності, виявлено зниження кількості норадреналіну в неокортексе і гіпокампі у віці 14 тижнів і зміни обміну серотоніну в гіпоталамусі, гіпокампі і неокортексе з віку 3 тижнів. Подібні порушення змісту і / або обміну нейротрансмітерів виражалися в зміні поведінки (підвищена збудливість), більш високому рівні кортикостерону плазми при попаданні в незнайоме оточення. У потомства зелених мавп, які зазнали однократному впливу дексаметазону в другій половині вагітності, за допомогою ядерного магнітного резонансу було виявлено зменшення обсягу гіпокампу на 20-30% у віці 20 місяців. Крім того, у цієї групи мавп був виявлений закономірно більш високий рівень кортизолу плазми (в ранкові, денні години, після стресу), ніж у контрольній групі.
Відповідно до існуючої теорії стан настройка гіпокамп-гіпоталамо-гіпофізарно-надниркової системи може бути порушена зміною кількості і / або афінності рецепторів глюкокортикоїдів в результаті дії механізму "програмування". Надалі це виробляти до більш вісокої, чем в нормі, секреції глюкокортікоїдів в дорослому віці. Трівала дія підвіщеного уровня глюкокортікоїдів спріяє розвитку артеріальної гіпертензії и збільшує ризики розвитку цукрового діабету 2-го типу. Сучасні дослідження на тваринах показують, що у потомства овець, які отримували недостатнє харчування в першій половині вагітності, отмечалалісь ослаблена відповідна реакція ГГГН системи на гіпоксію або на екзогенний кортикотропин-рилізинг гормон у внутрішньоутробному періоді, але посилений відповідь на ті ж стимули після народження.
КЛІТИНИ підшлункової залози
В даний час відомо, що під дією глюкокортикоїдів-клітини підшлункової залози плода піддаються апоптозу (програмованої загибелі) на певній критичній стадії внутрішньоутробного розвитку (у людини на терміні 28-32 тижні вагітності, у щурів на 7-14 добу післяпологового періоду) і замінюються - клітинами, характерними для дорослого організму. У цьому процесі бере участь система інсулін-подібних факторів росту.
ДЕКСАМЕТАЗОН І нейростероідов
Хоча дексаметазон широко використовується, як глюкокортикоїд, його ефекти не обмежуються дією тільки на класичні глюкокортікоїдниє рецептор. У дослідженнях, проведених багато років тому, було виявлено, що рецептор, що зв'язує дексаметазон в тканинах бика, не є класичним рецептором глюкокортіоідов. Не так давно був відкритий Х рецептор прегнана (PXR), який не пов'язував природні глюкокортикоїди (кортизол, кортикостерон), але пов'язував дексаметазон, прогестерон, прегненолон і деякі їх похідні. У вигляді димеру з рецептором 9-цис-ретиноєвої кислоти, PXR связиваетсясо специфічними сайтами ДНК, що складаються з двох повторюваних послідовностей. Потенційно активні нейростероідов, такі як аллопрегнанолон і тетрагідродеоксікортікостерон, утворюються в організмі під дією 5 -редуктазою, особливо під дією гідроксістероід-дегідрогеназ типів 2 і 3. Ген 5 -редуктази типу 2 транзиторно експресується в мозку щура в пізні терміни вагітності і в ранньому післяпологовому періоді. Експресія 3 -редуктазою індукується дексаметазоном, чинним нема на класичні рецептори глюкокортикоїдів. Утворені після індукції даних ферментів нейростероідов можуть впливати на багато аспектів диференціювання і дозрівання головного мозку, пов'язані зі становленням ендокринних і поведінкових функцій, взаємодіючи з рецепторами Габа, нікотиновими рецепторами ацетилхоліну, рецепторами N-метіласпартата і, можливо, з мембранними стероїдними рецепторами. Нейростероідов типу аллопрегненолона впливають на становлення барорефлекса. Ці дані відкривають нові горизонти для подальших досліджень впливу прийому глюкокортикоїдів на дозрівання функціональних систем плода.
ВИКОРИСТАННЯ ГЛЮКОКОРТИКОЇДІВ під час вагітності
За останні 20 років значно знизилася смертність серед недоношених новонароджених (24-26 тижнів), що багато в чому пов'язано з використанням в терапії глюкокортикоїдів при виникненні загрози передчасних пологів призначенням сурфактанту після народження. Якщо вдавалося уникнути передчасних пологів, то часто проводилися повторні курси введення глюкокортикоїдів. Виникають сумніви, не роблять чи повторювані ін'єкції глюкокортикоїдів несприятливого побічної дії на плід. Досліди на тваринах (вівця) показали, то повторні курси глюкокортикоїдів можуть призводити до затримки мієлінізації аксонів зорового нерва. Це дозволяє запідозрити можливе шкідливу дію глюкокортикоїдів на центральну нервову систему плода. У дітей, матері яких під час вагітності тривалий час отримували низькі дози глюкокортикоїдів, з метою зниження ризику розвитку проявів вродженого адреногенитального синдрому відзначалися певні порушення поведінки. Навіть за умови, що пренатальне лікування ГК ефективно в усуненні вірілізації у плодів жіночої статі з вродженою надниркової гіперплазією, тільки в одному з восьми випадків можна розраховувати на можливий позитивний ефект від такого лікування. З огляду на матеріал даного огляду, рекомендуються обмежити до мінімуму використання ГК під час вагітності.
ПИТАННЯ, залишилися без відповіді
Даний огляд підкреслює важливість того, що вагітна жінка повинна правильно харчуватися і бути в психологічно комфортному стані. Але багато проблем ще чекають свого вирішення.
Наскільки сильним повинен бути стресовий фактор, щоб привести до підвищеного ризику виникнення у потомства серцево-судинних і обмінних порушень? Дані визначення гормонів під час вагітності поки що недостатньо переконливі і суперечливі. Які точні терміни критичних періоди "програмування"? Скільки таких періодів протягом вагітності? Чи володіють і інші гормони кори надниркових залоз, а не тільки глюкокортикоїди, небажаною дією на плід? Чи можуть надавати шкідливу дію на плід мінералокортикоїди? Було показано, що хворі, що успадкували гиперальдостеронизм від матері, мали більш високі рівні альдостерону плазми, ніж ті, хто успадкував гиперальдостеронизм від батька. Передбачається, що ці люди піддавалися впливу підвищених рівнів альдостерону внутрішньоутробно. Нещодавно було показано зв'язок між кількістю вісцерального жиру і підвищеним рівнем альдостерону плазми. Збільшення кількості вісцерального жиру є частиною синдрому X, ризик розвитку якого в 10 разів вище в групі новонароджених з низькою масою тіла при народженні. Хронічний вплив альдостерону може бути причиною розвитку артеріальної гіпертензії. Альдостерон так само, як і глюкокортикоїди може змінювати експресію мРНК мінералокортикоїдних і глюкокортикоїдних рецепторів в гіпокампі.
Які механізми індукції патологічних змін? Чи є маркери виявлення дітей підвищеного ризику розвитку несприятливого програмування? Як потрібно лікувати дітей з низькою масою тіла при народженні, щоб знизити ризик розвитку артеріальної гіпертонії і / або обмінних порушень через 40 років?
Задати питання лікарю на форумі
Наскільки сильним повинен бути стресовий фактор, щоб привести до підвищеного ризику виникнення у потомства серцево-судинних і обмінних порушень?
Які точні терміни критичних періоди "програмування"?
Скільки таких періодів протягом вагітності?
Чи володіють і інші гормони кори надниркових залоз, а не тільки глюкокортикоїди, небажаною дією на плід?
Чи можуть надавати шкідливу дію на плід мінералокортикоїди?
Які механізми індукції патологічних змін?
Чи є маркери виявлення дітей підвищеного ризику розвитку несприятливого програмування?
Як потрібно лікувати дітей з низькою масою тіла при народженні, щоб знизити ризик розвитку артеріальної гіпертонії і / або обмінних порушень через 40 років?













