Углєв про ди, велика група органічних сполук, що входять до складу всіх живих організмів. Перші відомі представники цього класу речовин за складом відповідали загальній формулі CmH2nOn, тобто вуглець + вода (звідси назва); пізніше до У. стали відносити також їх численні похідні з іншим складом, що утворюються при окисленні, відновленні або введенні заступників.
Перетворення У. відомі з найдавніших часів, так як вони лежать в основі процесів бродіння, обробки деревини, виготовлення паперу та тканин з рослинного волокна. Тростинний цукор (сахарозу) можна вважати першим органічною речовиною, виділеним в хімічно чистому вигляді. Хімія У. виникла і розвивалася разом з органічною хімією ; творець структурної теорії органічних сполук А. М. Бутлеров - автор першого синтезу сахароподобние речовини з формальдегіду (1861). Структури найпростіших цукрів з'ясовані в кінці 19 ст. в результаті фундаментальних досліджень німецьких учених Р. Кіліаном і Е. Фішера , Заснованих на стереохімічних уявленнях Я. Г. Вант-Гоффа і блискуче їх підтвердили. У 20-і рр. 20 в. роботами англійського вченого У. М. Хоуорса були закладені основи структурної хімії полісахаридів. З 2-ої половини 20 ст. відбувається стрімкий розвиток хімії та біохімії У., обумовлене їх важливим біологічним значенням і базується на сучасній теорії органічної хімії і новітній техніці експерименту.
Класифікація та поширення вуглеводів. У. прийнято ділити на три основних групи: моносахариди, олігосахариди і полісахариди. Звичайні моносахариди являють собою поліоксил-альдегіди (альдози) або полпоксікетони (кетози) з лінійною ланцюгом атомів вуглецю (m = 3-9), кожен з яких (крім карбонильного вуглецю) пов'язаний з гідроксильною групою. Найпростіший з моносахаридів - гліцериновий альдегід - містить один асиметричний атом вуглецю і відомий у вигляді двох оптичних антиподів (D і L). Інші моносахариди мають кілька асиметричних атомів вуглецю; їх розглядають як похідні D- або L-гліцсрінового альдегіду і відносять відповідно до абсолютної конфігурацією при (т-1) -м атомі вуглецю до D- або L-pяду. Відмінності між моносахаридами в кожному ряду обумовлені відносною конфігурацією інших асиметричних центрів (див. ізомерія ). Характерна властивість моносахаридів в розчинах - здатність до мутаротації, тобто встановлення таутомерного рівноваги (див. таутомерія ) Між ациклической альдегидо- або кетоформой, двома п'ятичленних (фуранозной) і двома шестичленними (пиранозного) циклічними полуацетальнимі формами (див. Схему). Утворені піранози (як і фуранози) розрізняються конфігурацією (a або b) виникає при циклізації асиметричного центру у карбонільного атома вуглецю (на схемі позначений зірочкою).
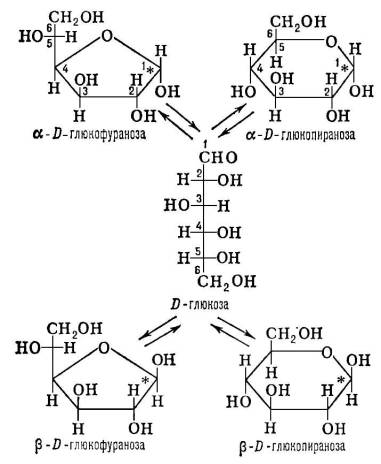
Співвідношення між таутомерними формами в рівновазі визначається їх термодинамічною стійкістю (для простих цукрів переважають пиранозного форми). Полуацетальний гідроксил різко відрізняється від інших гідроксильних груп моносахариду за здатністю до реакцій нуклеофільного заміщення. Такі реакції з різноманітними спиртами призводять до утворення глікозидів (Залишок спирту в глікозид називають агликоном). У тих випадках, коли агликоном служить молекула моносахариду, утворюються оліго- і полісахариди. При цьому кожен залишок моносахариду може мати пиранозного або фуранозной структуру, a - або b -конфігурації гликозидной зв'язку і бути пов'язаним з будь-якої з гідроксильних груп сусіднього моносахарида. Тому число розрізняються будовою полімерних молекул, які можна побудувати навіть тільки з одного моносахариду, величезна.
До найбільш типовим моносахаридам відносяться D - глюкоза , D- манноза , D- галактоза , D- фруктоза , D- ксилоза , L- арабиноза . До моносахаридів відносяться також: дезоксисахара, в молекулах яких один або кілька гидроксилов замінені атомами водню (L- paмноза , L- фукоза , 2-дезокси-D-pібоза); аміноцукри, в молекулах яких один або кілька гидроксилов замінені на аміногрупи (D-глюкозамін, D-галактозамин); поліспирти, або альдіти, що утворюються при відновленні карбонільних груп моносахаридів (сорбіт, маніт); уроновие кислоти , Тобто моносахариди, у яких первинна спиртова група окислена до карбоксильної; розгалужені цукру, що містять нелінійну ланцюг вуглецевих атомів (апіоза, L-cтрептоза); вищі цукру з довжиною ланцюга більше шести атомів вуглецю ( седогептулозо , сіалові кислоти ). За винятком D-глюкози і D-фруктози, вільні моносахариди зустрічаються в природі рідко. Зазвичай вони входять до складу різноманітних глікозидів, оліго- і полісахаридів і можуть бути отримані з них кислотним гідролізом. Розроблено методи хімічного синтезу рідкісних моносахаридів, виходячи з більш доступних.
Олігосахариди містять в своєму складі 2-10 моносахаридів, зв'язаних глікозіднимі зв'язками. Найбільш поширені в природі дисахариди сахароза , трегалоза , лактоза . Відомі численні глікозиди олі-госахарідов, до яких відносяться різні фізіологічно активні речовини (наприклад, флавоноїди , Серцеві глікозиди, сапоніни , Багато антибіотиків, гліколіпіди ).
Полісахариди - високомолекулярні, лінійні або розгалужені з'єднання, молекули яких побудовані з моносахаридів, зв'язаних глікозіднимі зв'язками. До складу полісахаридів можуть входити також заступники невуглеводної природи (залишки фосфорної, сірчаної і жирних кислот). У свою чергу ланцюга полісахаридів можуть приєднуватися до білків з утворенням гликопротеидов . Окрему групу становлять біополімери, в молекулах яких залишки моно- або олігосахаридів сполучені один з одним не глікозіднимі, а фосфодіефірнимі зв'язками; до цієї групи належать тейхоевие кислоти з клітинних стінок грампозитивних бактерій, деякі полісахариди дріжджів, а також нуклеїнові кислоти , В основі яких лежить полірібозофосфатная (РНК) або полі-2-дезоксірібозофосфатная (ДНК) ланцюг.
Фізико-хімічні властивості вуглеводів. Завдяки великій кількості полярних (гідроксильних, карбонильной і ін.) Груп в молекулах моносахаридів вони добре розчинні у воді і нерозчинні в неполярних органічних розчинниках (бензолі, петролейном ефірі та ін.). Здатність до таутомерним перетворенням зазвичай ускладнює кристалізацію моносахаридів. Якщо такі перетворення неможливі, як в глікозидах або олігосахариди типу сахарози, речовини кристалізуються легко. Багато глікозиди з малополярни Аглікон (наприклад, сапоніни) виявляють властивості поверхнево-активних сполук. Полісахариди є гідрофільними полімерами, молекули яких здатні до асоціації з утворенням високов'язких розчинів (рослинної слизу , гіалуронова кислота ); при певному співвідношенні вільних і асоційованих ділянок молекул полісахариди дають міцні гелі (Агар, пектинові речовини ). В окремих випадках молекули полісахаридів утворюють високоупорядоченние надмолекулярних структури, нерозчинні у воді ( целюлоза , хітин ).
Біологічна роль вуглеводів. Роль У. в живих організмах надзвичайно різноманітна. У рослинах моносахариди є первинними продуктами фотосинтезу і служать вихідними сполуками для біосинтезу різноманітних глікозидів, полісахаридів, а також речовин ін. класів (амінокислот, жирних кислот, поліфенолів і т.д.). Ці перетворення здійснюються відповідними ферментними системами, субстратами для яких служать, як правило, багаті енергією фосфорильовані похідні цукрів, головним чином нуклеозіддіфосфатсахара. У. запасаються у вигляді крохмалю у вищих рослинах, у вигляді глікогену в тварин, бактеріях і грибах і служать енергетичним резервом для життєдіяльності організму (див. бродіння , гліколіз , окислення біологічне ). У вигляді глікозидів в рослинах і тваринах здійснюється транспорт різних продуктів обміну речовин. Численні полісахариди або більш складні углеводсодержащие полімери виконують в живих організмах опорні функції. Жорстка клітинна стінка у вищих рослин побудована з целюлози і геміцелюлози, у бактерій - з пептидоглікану; в побудові клітинної стінки грибів і зовнішнього скелета членистоногих бере участь хітин. В організмі тварин і людини опорні функції виконують сульфатованих мукополісахариди сполучної тканини, властивості яких дозволяють забезпечити одночасно збереження форми тіла і рухливість окремих його частин; ці полісахариди також сприяють підтримці водного балансу і виборчої катіонної проникності клітин. Аналогічні функції в морських багатоклітинних водоростях виконують сульфатованих галактани (червоні водорості) або складніші сульфатованих гетерополі-цукориди (бурі і зелені водорості); в зростаючих і соковитих тканинах вищих рослин аналогічну функцію виконують пектинові речовини. Особливо важливу і до кінця ще не вивчену роль відіграють складні У. в освіті специфічних клітинних поверхонь і мембран. Так, гліколіпіди - найважливіші компоненти мембран нервових клітин, ліпополісахариди утворюють зовнішню оболонку грамнегативних бактерій. У. клітинних поверхонь часто визначають явище імунологічної специфічності, що строго доведено для групових речовин крові і ряду бактеріальних антигенів . Є дані, що вуглеводні структури беруть участь також в таких високоспецифічних явищах клітинної взаємодії, як запліднення, «впізнавання» клітин при тканинної диференціації і відторгненні чужорідної тканини і т.д.
Практичне значення вуглеводів. У. становлять велику (часто основну) частину харчового раціону людини (див. харчування ). У зв'язку з цим вони широко використовуються в харчовій і кондитерській промисловості (крохмаль, сахароза, пектинові речовини, агар). Їх перетворення при спиртовому бродінні лежать в основі процесів отримання етилового спирту, пивоваріння, хлібопечення; ін. типи бродіння дозволяють отримати гліцерин, молочну, лимонну, глюконовую кислоти і ін. речовини. Глюкоза, аскорбінова кислота, серцеві глікозиди, углеводсодержащие антибіотики, гепарин широко застосовуються в медицині. Целюлоза є основою текстильної промисловості, отримання штучного целюлозного волокна, пластмас (див. Етроли ), Вибухових речовин (див. нітрати целюлози ) та ін.
Найважливіші питання хімії та біохімії У.- удосконалення методів встановлення будови і синтезу природних В., з'ясування зв'язку між їх структурою і функцією в організмі, а також шляхів біосинтезу - розробляються хімічними і біохімічними науковими центрами поряд з ін. Актуальними проблемами органічної хімії, біохімії та молекулярної біології. Дослідженням тільки в області У. присвячені спеціалізовані міжнародні видання: щорічник «Advances in Carbohydrate chemistry and biochemistry» (c 1945) і журнал «Carbohydrate research» (c 1965). см. також статті бродіння , з'єднання природні , вуглеводний обмін , фотосинтез .
Літ .: Хімія вуглеводів, М., 1967; Методи хімії вуглеводів, пров. з англ., М., 1967; Глікопротеїни [т. 1-2], пров. з англ., М., 1969; Carbohydrates, ed. by G. О. AspinalI, L. - Baltimore, [1973]; Industrial gums, eds. RL Whistler and JN Bemiller, 2 ed., NY - L., 1973.
А. І. Усов.

Мал. до ст. Вуглеводи.













